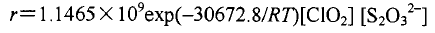ClO2
稳定性二氧化氯溶液
硫代硫酸钠还原二氧化氯的动力学
实验部分
试剂及仪器
C102,在10%H2SO4的介质中由NaC102/K2S2O8体系发生,纯度为99.8%以上,除去空气并溶解于 冷水,保存于棕色瓶中,低温密封避光保存,作为储备液。每天测定H 、C1一、C102一、C103-杂质,一个 月内未发现这些杂质,使用时,准确标定并稀释至实验所需浓度。
硫代硫酸钠、碘和NaC10 均为分析纯以上纯度。硫代硫酸钠和碘溶液当天配制使用,实验用水为三 次蒸馏水:所用溶液的离子强度采用NaC10 调节到0.5 mo1.L~。
采用硼酸.氢氧化钠(硼酸盐缓冲液)作缓冲液调节溶液的pH值为8.55
Dionex 2010i离子色谱仪:Hi.Tech SF.61型动力学停流仪;PH.3c型精密酸度计:精密恒温槽;Agilent8453型分光光度计。
动力学研究方法
动力学研究在Hi.Tech SF.61型动力学停流仪反应器上进行。以pH值为8.55的硼酸盐缓冲液控制 C102与Na2S2O3的pH值,加入NaC104调节离子强度,其浓度为0.5 mol・L~,然后将二氧化氯和硫代硫 酸钠的反应液分别加入到两根试样注射器中([S2032-】0控制在(0.235-0.688)X 10一mol・L~、[C102】0控制在 (0.759~1.840)X 10一mol-L ),设定好温度,通过控制蠕动泵将反应物溶液迅速推入反应室,在大约lms 时间内停止流动并依靠扩散混合发生反应;混合后进入检测器,在300~420 am的l0个测定波长进行动 力学时间扫描,同时由微机采集和处理来自检测系统的UV-Vis吸收信号,对得到的动力学曲线进行拟合, 进而求出相应的反应动力学参数。
分析方法
(1)氯化物的测定采用连续碘量法。
(2)硫化物的测定采用离子色谱法。色谱条件:CDM.2电导检测器:Polyspher ICAN.1阴离子分析 柱(4 mmX 100 mm);淋洗液:2.5 X 10一mo1.L一 对羟基 丁酸和水/甲醇溶液(1:9, ,用0.01 mo1.L一 的N,N . 二乙基乙醇胺调节淋洗液的pH 值为9.27:淋洗流速: 1.5 mL・min~;进样体积:25 :柱温:313 K。
结果与讨论
反应过程中主要物质的吸收光谱
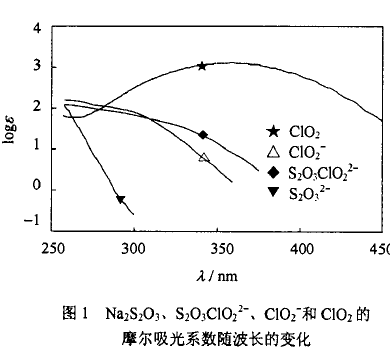
图l中表明了硫代硫酸钠、S2O3C1022_、以及亚氯酸 钠和二氧化氯等物质的摩尔吸光系数随波长变化的关 系。其中,硫代硫酸钠、以及亚氯酸钠和二氧化氯是实 验中测定的;$203C1022-的摩尔吸光系数与波长关系为 Istvdn等人在研究硫代硫酸钠.亚氯酸钠反应体系中发现并估算出的。图1中的纯吸收光谱数值是计算硫代硫酸钠还原过量二氧化氯的反应过程物质浓度变化依据。
过量二氧化氯与硫代硫酸钠反应动力学参数的确定
反应级数及速率常数的测定
在pH=8.55、 =298 K的实验条件下,由分光光度计设定10个上述波长进行时间扫描测定。
图2描述了在360 nin下检测的反应过程中吸光度随时间变化的曲线(其他波长下的曲线未示出),表 现出反应瞬态的吸收图谱变化关系,曲线上各点的吸光度值是由反应过程中各物质(图1所示)吸收光谱 重叠而得到的。
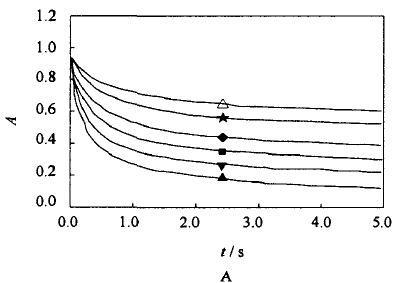
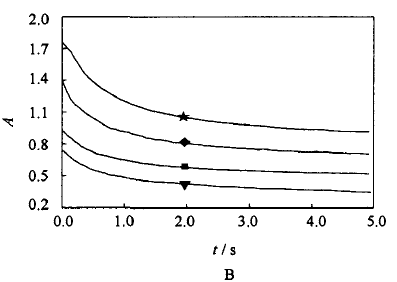
图2 不同的[ClO2】o/[s2032-]o,测得360 nm处吸光度随时间的变化(pH8.55、298 K)
根据Lambert―Beer定律,由图1中各个物质的摩尔吸光系数以及图2中的吸收光谱值进行四元线性 拟合,设其回归模型为:总的吸光度值 = lCl+ 2c2+ 3c3+ 4C4+C0+ ,其中,Cl~4分别为硫代硫酸钠、S2O3CIO22-、亚氯 酸钠和二氧化氯的浓度; l 分别为它们的摩尔吸光系数数值,Co为常数项。采用excel中的线性拟合 函数LINEST来进行拟合回归分析,得到的回归系数el 即为某个反应时间的体系中各物质浓度。
结 论
(1)采用离子色谱法和连续碘量法研究了硫代硫酸钠还原过量二氧化氯的化学计量关系,得出其化 学反应方程式为:S2O32-十4C102+3H2O-->2SO42一十3 CIO2-+C1一十6H+
(2)采用停流技术,根据反应瞬间吸收光谱值测出了过量二氧化氯.硫代硫酸钠的反应动力学参数。结果表明,在pH 8.55和298K的条件下,硫代硫酸钠还原过量二氧化氯的反应速率常数k值为4 5208 ×10 L・mol-1"S~;反应活化能Ea为30.67 kJ・mol~;表明在一般的水处理研究中,硫代硫酸钠作为二氧化氯的猝灭剂是合理的。
(3)在pH 8.55的条件下,过量二氧化氯-硫代硫酸钠的反应对于二氧化氯和硫代硫酸钠均为一级,总 反应级数为二级,其总的反应动力学方程为: