
ClO2
稳定性二氧化氯溶液
二氧化氯的制备方法
1. 1 二氧化氯的制备
1. 1. 1 化学法
(1) R5 法或称凯斯汀(KESTING) 法:
该法以HCI 还原NaClO3 或CA(CLO3 ) 2 ,制得ClO2
和NaCI ,NaClO3 与32 %盐酸同时加入第一反应器,溢流
通过至第六反应器,从反应器通入空气,搅拌反应液,
经稀释生成C1O2 气体,经吸收塔用冷水吸收成ClO2 水
溶液,未被吸收的Cl2 用碱液吸收制得NaClO3 溶液:
NaClO3 + 2HCI ClO2 + 0. 5 Cl2 + NaCl + H2O
NaClO3 + 6HCI 3Cl2 + NaCl + 3H2O
副产物NaCl 回收作为电解制NaClO3 的原料盐水, 该方法增加气体分离操作和处理副产物NaCl 和Cl2 的 生产设备,投资大,ClO2 收率只有87 %左右,而且反应 温度高,多级反应,反应过程不易控制,可用湿性硫磺、锰、铂离子或氨基酸作催化剂,能减少NaClO3 的损耗。
日曹法改用Ca (ClO3) 2 代替NaClO3 ,与盐酸作用, 副产物是CaCl2 而不是NaCl 。
Ca (ClO3) 2 + 4HCl 2ClO2 + Cl2 + CaCl2 + 2H2O
(2) R6 法
此法典型的有加拿大凯密迪(Chemetics) 公司开发 的Inte - grated 系统,生产除ClO2 发生系统外,还有电解 和HCl 合成两个系统,系统密闭循环,生产时仅需补充 部分原料Cl2 。钛制ClO2 发生器分隔成9 个反应室,各 反应室分别通入空气,稀释反应生成的ClO2 和Cl2 并将 其带走,在微负压下工作。该法优点:系统是一个全液 体封闭工艺,生产过程无固形物料。首次开机时加足 盐水后不再加入盐水,仅需补充部分Cl2 与马蒂逊法等 相比其运行费用要低得多,系统不使用昂贵的银、锰催 化剂,无NaClO3 损失,没有副产品排放,对环境污染少, 发生器在微负压下工作,避免了在高真空度操作所需 要的设备及操作费用。该法的缺点:系统包括了HCl 合成、NaClO3 电解部分,其一次性投资较大,三大系统 互相联系,互相制约,一个系统的故障可能导致其他系 统生产运行状况不稳定,系统启动时间长,需要1 - 2h 才能正常运行,停机程序也复杂。
(3) R7 法
此法20 世纪80 年代初实现工业化,和R6 法比较
一样是组合工艺,主要目的就是减少Cl2 的产生,并加
以利用,无副产物的产生,但投资大、耗电多、收率低。
反应式:
2NaClO3 + 2HCl + H2S4O 2ClO2 + Cl2 + 2H2O +
Na2SO4
Cl2 + SO2 + 2H2O 2HCl + H2SO4
总反应式:2NaClO3 + SO2 2ClO2 + Na2SO4
(4) 马蒂逊法(Mathienson) 法(R1 法)
以SO2 为还原剂,在硫酸介质中还原NaClO3生成ClO2 。
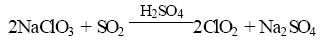
反应时通入的SO2 气体太少反应不完全,ClO2与Cl2比值小,但通入SO2过多也不利,应保持ClO2:Cl2=10~20 时所需SO2量,反应液硫酸浓度8mol/l左右,硫酸过浓会使主反应和副反应的速度均加快,副产Cl2增 多,硫酸浓度过低使反应介质酸度不够,影响ClO2浓度。由于利用回收废酸,反应液中含有部分Na2SO4,若 浓度过高会造成NaHSO4・H2O 结晶析出,影响操作,并气体产物中Cl2 增加,一般控制Na2SO48.5g/l以下,反 应液中原料NaClO3浓度控制在260g/ l左右,含量过时在1O ℃以下会析出NaClO3 结晶。该法制得的ClO2 比 盐酸纯,副产Cl2少。但以SO2 作还原剂, 产物中有SO2,还有Cl2杂质,使ClO2纯度不高,收率只有90 %。 新马蒂逊法采用SO2 法和NaCl法相结合的办法,在马蒂逊法的基础上另加原料NaClO3 量的5~20 %NaCl ,可 使ClO2产率提高到95~97%。ClO2 反应器加以改进,反应物料通过分配装置由喷射泵入反应器内,每个反 应器都附有真空泄气阀,利用它来间断反应物料的加料,避免爆炸和利于控制加料。
另一种对马蒂逊法的改进是大曹法,将H2SO4加到废酸中去,然后冷却到0 ℃使生成的NaHSO4・H2O分离出去。
(5) R2 法
采用NaCI 还原NaClO3 。将NaClO3 和NaCl的摩尔比为1:1. 05 混合水溶液加入反应器,再与98 %H2SO4 于35~55 ℃进行反应,生成的ClO2 与Cl2 由通入空气驱出,混合气体进入ClO2 吸收塔,用冷水对流吸收,生成 ClO2水溶液,而未溶的Cl2(12~13 %) 则进入Cl2 吸收塔,用碱液吸收生成NaClO 或用石灰乳吸收制成漂白 液出售。汽提塔排出的废液,主要是Na2SO4 和H2SO4 ,还有少量NaCl和NaClO3,可供牛皮纸浆生产之用。总反应式:
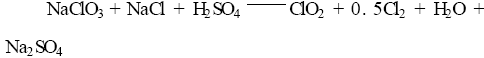
析出结晶后的母液循环使用,可使酸耗降低,每生产1KgClO2 耗98%H2SO4 约1.5Kg。R2法收率较高,生 产过程简单,设备投资少,但耗费大量H2SO4 ,产生大量废液, 产品中含Cl2占整个气体1/3,且产生大量Na2SO4,通过下列方法将Cl2转为ClO2。
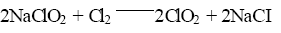
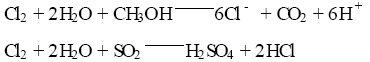
这些方法反应很缓慢,为提高反应速度要使用催化剂和提高反应介质的酸度,要增加成本,设备腐蚀更大。用甲醇作还原剂,产品在漂白应用中由于副反应形成的甲醛和甲酸以及没有反应完的甲醇与伴随漂白 而来的醛、酸和酯可能发生反应,产生氯化的有机化合物。因R2法基础上发展的R3法、R3H法、R5法、SVP法等方法可降低副产Na2SO4的生成。
1. 1. 2 电解法
电解法是以氯酸钠或氯化钠为原料,采用隔膜电解技术制取ClO2,所用的电解液可以是食盐溶液、亚氯 酸盐溶液和氯酸盐。电解过程中,在阴极制得烧碱溶液和氢气,阳极获得ClO2 、氯气、过氧化氢及臭氧的混合物。美国虎克公司和Tetravalent 公司分别获得该项技术专利。
电解法制取ClO2设备复杂,生产成本高,产气量不稳定,故障率高,耗电量大,影响了该法的推广和应用。 国内有四川雅安中竹纸业有限责任公司用联合电解法生产ClO2 。
1. 2 稳定性二氧化氯的制备
由于ClO2具有易爆、易分解、强腐蚀的特点,目前压缩或贮存ClO2 的一切尝试在商业上均未能成功。稳 定性ClO2是人们在研制ClO2的基础上,为解决其生产、使用过程中的安全性、方便性,而将ClO2 稳定在惰 性溶液或某些固体物质中形成一定浓度有效ClO2的产品。目前该产品主要生产工艺是氯酸盐或亚氯酸盐经 酸化,产生高纯度ClO2气体,经空气或惰性气体稀释后,通入稳定液中吸收而成。通常是将ClO2 通入碳酸 钠、过碳酸钠、硼酸盐等惰性溶液中,使之达到饱和制得含ClO2浓度2.0 %以上的液体稳定ClO2 产品。使用 时用酸活化即可。现还开发了固体稳定性二氧化氯,将水溶液中的ClO2吸附在硅酸钙、分子筛等多孔性物 质上制得固体稳定性二氧化氯产品。有时用明胶或琼脂为基质配以其它辅料为载体,制成固体缓释型ClO2产品。稳定性二氧化氯无色、无味、无毒、无腐蚀性,不 易燃,不挥发,不分解,性质稳定,便于贮存和运输,在 - 5~95 ℃下能贮存2年之久,使用安全方便易行。
总之,我国目前在ClO2 的生产技术和应用下都还有许多研究工作需要去做。建议我国相关部门、企业、大专院校加强ClO2 的开发,推动ClO2 在我国的广泛应用,前景十分广阔。相信随着ClO2 的制备技术的成熟和人类对自身健康、生态环境的日益关心,将可实现 ClO2 产品的低成本、大规模化生产,开发出更多的应用领域,造福人类。